添加日期:2018年7月24日 阅读:1435
在过去几年中,被公布出来的医疗器械召回信息中,涉及的绝大部分是外资企业。但自去年开始,涉及本土医疗器械企业的召回信息开始不断出现,并且有增加的趋势。
7月20日,上海市食药监局发布该市医疗器械企业召回报告,印证了这一点:国产召回数量在增加。以下为报告主要内容:
2018年上半年,上海市食品药品监督管理局共发布了165项医疗器械企业主动召回信息。按产品种类,有源类产品100项、无源类产品37项、体外诊断试剂产品28项;按产品缺陷严重程度高低,一级召回3项、二级召回52项、三级召回110项。
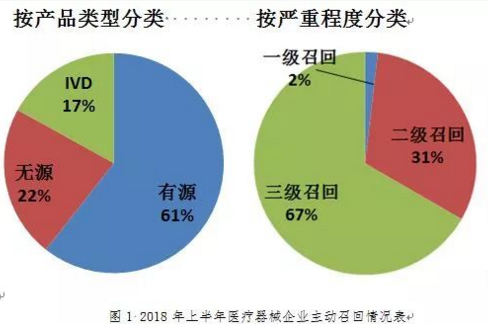
召回情况总体分析
上半年发布的主动召回数量,同比去年增长了66.7%。从召回企业主体分析,国产医疗器械主动召回量增多,上半年共有11个国产医疗器械主动召回。
其中,因监督抽检不合格发起的召回行动2个,因飞行检查发现缺陷发起的召回行动2个,监督抽检和飞行检查中发现的产品缺陷企业启动了主动召回,医疗器械监督抽检、飞行检查和主动召回工作形成了有效联动,初步形成监管合力。
召回原因分析
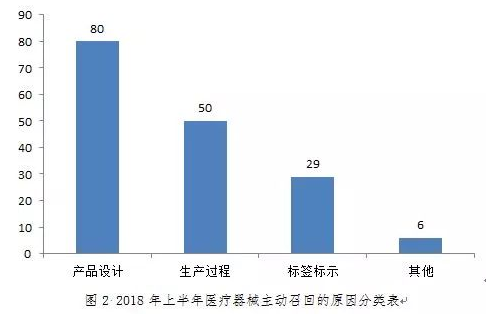
2018年上半年,造成主动召回的原因主要有产品设计缺陷、生产过程控制缺陷问题、标签标示错误等几方面原因。
产品设计缺陷造成的召回事件约占总数的48%,其中产品软件缺陷导致的产品故障占多数;生产过程控制缺陷导致的召回事件约占总数的30%,由于装配错误、包装不达标等原因造成了终产品未能完全实现产品的预期用途。
另有标签标示错误造成的召回占总数的18%,主要原因是中文标签上的注册证号等信息有误;召回更新等其他类别的召回事件占总数的4%。
召回风险提示
一是关注血糖试纸缺陷风险。上半年的血糖试纸一级召回原因是葡萄糖检测试纸(酶法)酶含量较低,影响测定结果,进而影响患者用药,特别是孕妇用药错误对胎儿的影响。
二是关注无菌产品的细菌内毒素风险。上半年的一例一级召回中,涉及产品包装环箍上存在可检出水平的细菌内毒素,临床使用可能发生交叉感染。
三是关注有源植入物因供电故障引发的风险。一例心脏复律除颤器产品的召回中,企业通过基于产品自身的电池性能检测的固件升级,用于对电池性能异常进行报警。
四是关注标签标识错误可能引发的合规风险。2018年上半年医疗器械主动召回事件中,标签标示错误的数量有所上升,同比去年同期上升了93%,主要表现为注册证编号信息错误等情况。
目前,相关医疗器械企业已对可能的缺陷产品进行了调查评估,并采取了相应的纠正预防措施。
文章来源:上海食药监局
1.凡本网注明“来源:1168医药招商网”的所有作品,均为广州金孚互联网科技有限公司-1168医药招商网合法拥有版权或有权使用的作品,未经本网授权不得转载、摘编或利用其它方式使用上述作品。已经本网授权使用作品的,应在授权范围内使用,并注明“来源:1168医药招商网http://www.1168.tv”。违反上述声明者,本网将追究其相关法律责任。
2.本网转载并注明自其它来源(非1168医药招商网)的作品,目的在于传递更多信息,并不代表本网赞同其观点或和对其真实性负责,不承担此类作品侵权行为的直接责任及连带责任。
3.其他媒体、网站或个人从本网转载时,必须保留本网注明的作品第一来源,并自负版权等法律责任。
4.如涉及作品内容、版权等问题,请在作品发表之日起一周内与本网联系,否则视为放弃相关权利。联系邮箱:1753418380@qq.com。

【适用范围】用于缓解颈、肩、腰、腿及闭合性软组织疼痛、肿胀等不适症状人群的物理冷敷。【使用方法】外用。将本品适量直接涂抹于不适部位,轻轻按摩2-3分钟,每日2-3次。

【适用范围】用于缓解颈、肩、腰、腿及闭合性软组织疼痛、肿胀等不适症状人群的物理冷敷。【使用方法】外用。将本品适量直接涂抹于不适部位,轻轻按摩2-3分钟,每日2-3次。
 粤公网安备 44011102000390号
粤公网安备 44011102000390号